Introdução:
Os
modelos atômicos são modelos que vêm sendo desenvolvidos há séculos por
cientistas que procuravam demonstrar o formato de um átomo e como ele funciona.
Modelo Atómico de Dalton:
John Dalton, no séc. XIX (a partir de 1803), retomou a ideia dos átomos como constituintes básicos da matéria. Para ele os átomos seriam partículas pequenas, indivisíveis e indestrutíveis .
Modelo Atómico de Dalton:
John Dalton, no séc. XIX (a partir de 1803), retomou a ideia dos átomos como constituintes básicos da matéria. Para ele os átomos seriam partículas pequenas, indivisíveis e indestrutíveis .

Modelo atómico de Dalton
Os principais características da Teoria Atômica de Dalton são:
-a matéria é formada por partículas
extremamente pequenas chamadas átomos;
-os átomos são esferas maciças,
indestrutíveis e intransformáveis;
-átomos que apresentam mesmas
propriedades (tamanho, massa e forma) constituem um elemento químico;
-átomos de elementos diferentes possuem
propriedades diferentes;
-os átomos podem se unir entre si
formando "átomos compostos";
uma reação química nada mais é do que a
união e separação de átomos.
Modelo Atômico de Thomson:

Cada átomo seja composto de uma parte positiva
grande e pesada mais uma quantidade de elétrons menores e mais leves.
Especificamente, o modelo do átomo de Thomson era uma esfera de carga elétrica positiva
na qual estavam contidos alguns elétrons.
Modelo Atômico de Rutherford:
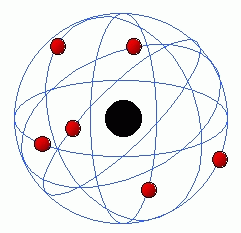
O cientista neozelandês Ernest
Rutherford, recorrendo à realização de uma esperiência, que consistia no
bombardeamento com particulas numa lâmina de ouro (tendo cerca de 10000 átomos
de espessura), permitiu-lhe concluir que a maior parte dos átomos era
espaço vazio e no interior desse mesmo átomo, existia uma zona central com
carga positiva, onde estaria concentrada toda a massa do mesmo. Deste modo
Ernest Rutherford imaginou os átomos constituidos por um núcleo de pequenas
dimensões, com carga positiva, onde se concentra a massa geral do átomo e por
electrões com carga elétrica negativa que se movimentam à volta do núcleo.
Assim surgiu o primeiro planetário do átomo (séc. XX).
Modelo Atômico de Bohr:
O cientista Niels Bohr, completou o modelo
átomico de Rutherford, com as seguintes ideias (1913):
- os elctrões, que são as partículas do átomo
com carga negativa, movem-se à volta do núcleo em órbitas circulares, tal como
fazem os planetas à volta do sol, no sistema solar;
- a cada órbita corresponde um determinado
nível de energia;
- os electrões que possuem mais energia movem-se
em órbitas mais afastadas do centro, isto é, do núcleo, e os electrões com
menos energia encontram-se a circular em órbitas perto do núcleo do átomo.
Modelo Atômico Atual:
Actualmente foi posta de parta a ideia das
órbitas circulares à volta do núcleo para os electrões.
Hoje, defende-se a ideia que os electrões dos
átomos movem-se de forma desconhecida e com uma velocidade elevadíssima,
formando uma nuvem que foi designada por: nuvem electrónica.
A nuvem elctrónica é mais densa no centro,
isto é perto do núcleo, onde é mais provável ser encontrado um electrão e menos
densa longe do núcleo, onde é mais improvável ser encontrado um electrão.

Núcleo: protões
(carga positiva) e neutrões (carga neutra)
Nuvem
electrónica: electrões (carga negativa)
Bem galera é isso,não esqueçam de comentar se te ajudei,e ser membro pra mais explicações..
Nenhum comentário:
Postar um comentário